Propiedades de la materia, mezclas, características, y Leyes de la combinación Química
Introducción
Definición
La química es la ciencia que estudia la composición, estructura y propiedades de la materia ya sea en forma de elementos, compuestos, mezclas u otras especies, así como los cambios que esta experimenta durante las reacciones. Además la química se ocupa de las agrupaciones supratómicas, como son los gases, las moléculas, los cristales y los metales, estudiando su composición, propiedades estadísticas, transformaciones y reacciones. A su vez incluye la comprensión de las propiedades e interacciones de la materia a escala atómica. Para captar la lógica de la reciente evolución de la química, hay que retroceder en el tiempo y dar un salto hacia varios eones atrás.Historia
| Mineral de Ocre |
 |
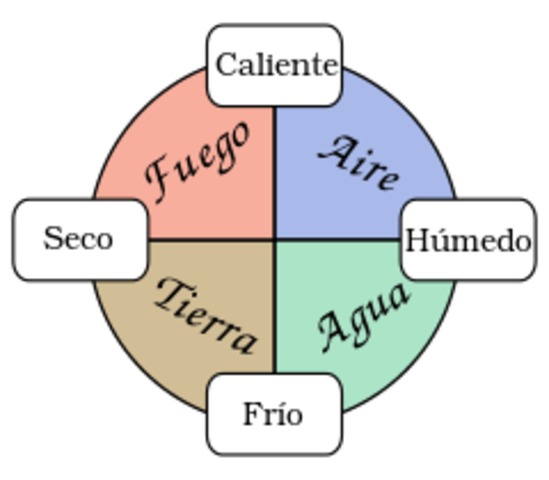
primarios: tierra, aire, fuego y agua, sobre los cuales actúan dos fuerzas opuestas y activas (amor y odio, o afinidad y antipatía) que terminan por combinarlos o separarlos en formas infinitamente variadas. Los postulados anteriores fueron adsorbidos por la alquimia y en base a estos se hicieron algunos avances en lo que hoy llamamos como química, descubrieron bastantes compuestos que luego al combinarlos con otros podían crear productos con una utilidad, además varios de los instrumentos y recipientes de vidrio que hoy en día se usan, vienen de la época alquímica, aunque esta disciplina no avanzaría en la comprensión real de la realidad sin un método de experimentación riguroso como es el método científico.
 |
| Jan Baptista van Helmont |
 |
Pero el punto decisivo en donde la química se separo de la alquimia fue en 1661 con Robert Boyle publicando “The Sceptical Chymist”, un tratado donde se hace la diferenciación entre las pretensiones subjetivas de la alquimia y los descubrimientos científicos empíricos de la nueva química. Él formuló la ley de Boyle, rechazó los «cuatro elementos» y propuso una alternativa mecánica de los átomos y las reacciones químicas las cuales podrían ser objeto de experimentación rigurosa, demostrándose o siendo rebatidas de manera científica.
 |
| Tabla de Mendeléyev |
hasta que llego el modelo de Mendeléyev, en donde ordenaba los elementos en base a su peso atómico, así como en base a sus propiedades químicas similares; dicho ordenamiento fue tan potente que incluso su creador dejaba huecos en la tabla que para él eran elementos que no se habían descubierto todavía, y así fue, los elementos con posiciones similares tenían propiedades similares, haciendo que la tabla de Mendeléyev sea la usada aun hoy en día.
 |
| Modelo deDalton |
La química en sus primeros años tenía mucho trabajo por hacer, era una ciencia joven y se hacían descubrimientos casi a diario, pero con el tiempo se empezó a buscar mas a fondo como funcionaba desde raíz; comprender como los diferentes átomos se combinaban, hacer eso traería un crecimiento exponencial en las posibilidades de la química, y primer paso es describir con claridad el elemento base, el átomo, el primero modelo atómico lo dio John Dalton en 1803, que rescata la idea de átomo o unidad indivisible de la materia de los griegos Leucipo y Demócrito. Dicho modelo no constaba de muchas componentes, se pensaba que el átomo era algo sólido, inmutable e indivisible.
 |
| Modelo budín de pasas |
Pero en 1897, J. J. Thomson, con experimentos de rayos catódicos descubrió un componente del atomo, el electrón, un paticula con muy poca masa y con carga negativa, es decir, si el electron tenia carga negativa debería haber una carga positiva para mantener neutra la carga del atomo, entonces el modelo atómica cambio a lo que hoy en día llamamos “El modelo budín de pasas”, en donde los electrones están adheridos al átomo
 |
| Modelo de Bohr |
.png) |
| Modelo de Rutherford |
La comprensión del átomo dio su siguiente paso con una serie de experimentos de dispersión, a cargo del físico Ernest Rutherford, en la Universidad de Mánchester, descubrió la estructura interna del átomo y la existencia del protón, clasificando y explicando los diferentes tipos de radiactividad; luego El trabajo de Rutherford en la estructura atómica fue mejorado por sus estudiantes, Niels Bohr y Henry Moseley, y por último en 1923 James Chadwick descubrió el neutrón anteriormente predicho por Rutherford para contrarrestar la repulsión electroestática de los protones en el núcleo y evitar la desintegración del átomo. Este modelo es el más enseñado hoy en día, en donde los electrones se mueven alrededor del núcleo. Pero queda algo obsoleto bajo la comprensión actual del átomo, le hace falta algo más… Cuántico
 |
| Orbitales Atomicos |
| |
Materia
La principal labor de la química es estudiar los cambios de la materia, dichos cambios pueden ser de dos tipos, Físicos (si no está relacionado con enlaces químicos), o Químicos (Si los enlaces químicos están involucrados)
Propiedades Químicas
 pH. La corrosividad de los ácidos y la
causticidad de las bases tiene que ver con el pH de la materia, o sea, su nivel
de acidez o alcalinidad, su capacidad de donar o recibir electrones cuando está
en contacto con ciertos materiales, como los metales o como la materia
orgánica.
pH. La corrosividad de los ácidos y la
causticidad de las bases tiene que ver con el pH de la materia, o sea, su nivel
de acidez o alcalinidad, su capacidad de donar o recibir electrones cuando está
en contacto con ciertos materiales, como los metales o como la materia
orgánica.
- Reactividad. De acuerdo a su constitución atómica, la materia puede ser más o menos reactiva, es decir, más o menos propensa a combinarse con otras sustancias. En el caso de las formas más reactivas, como los metales cesio (Ce) y francio (Fr), es raro verlos en formas puras, casi siempre son parte de compuestos con otros elementos. Los llamados gases nobles o gases inertes, en cambio, son formas de la materia con bajísima reactividad, que casi no sufren reacción con ninguna otra sustancia.
- Inflamabilidad. Algunas sustancias pueden
inflamarse, es decir, generar una explosión que
 libera calor y produce llamas,
en presencia de una fuente de calor o en una reacción con otras sustancias. A
dicha materia se la denomina inflamable (por ejemplo, la gasolina).
libera calor y produce llamas,
en presencia de una fuente de calor o en una reacción con otras sustancias. A
dicha materia se la denomina inflamable (por ejemplo, la gasolina).
- Oxidación. Es la pérdida de electrones de un átomo o ion cuando reacciona frente a un determinado compuesto.
- Reducción. Es la ganancia de electrones de un átomo o ion cuando reacciona frente a un determinado compuesto.
Propiedades físicas
- Temperatura. Es el grado de calor que presenta la materia en un momento, que generalmente se irradia hacia el entorno cuando una sustancia tiene mayor temperatura que su entorno. La temperatura es el grado de energía cinética que presentan las partículas de un material.
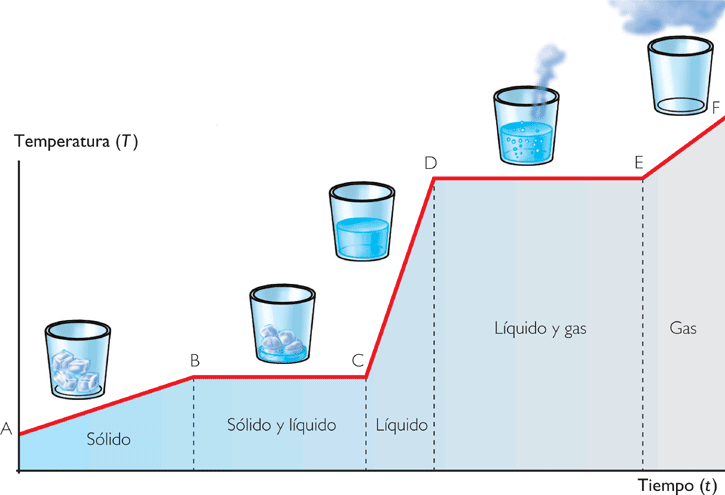
- Estado de agregación. La materia puede aparecer en tres “estados” o estructuras moleculares determinadas por su temperatura o la presión a la que esté sometida. Estos tres estados son: sólido (partículas muy juntas, baja energía cinética), líquido (partículas menos juntas, energía cinética suficiente para que fluya la materia, sin separarse del todo) y gaseoso (partículas muy alejadas, alta energía cinética).
- Conductividad o conductividad. Existen dos formas de conductividad: la térmica (calor) y la eléctrica (electromagnetismo), y en ambos casos se trata de la capacidad de los materiales de permitir el tránsito de la energía a través de sus partículas. Los materiales de alta conductividad se conocen como conductores, los de baja conductividad como semiconductores y a los de nula conductividad como aislantes.
- Punto de fusión. Es la temperatura a la que un sólido se transforma en líquido a la presión de 1 atm.
- Punto de ebullición. Es la temperatura a la cual la presión de vapor de un líquido se iguala a la presión que existe alrededor del líquido. En este punto el líquido se transforma en vapor. Cuando la presión de vapor del líquido se iguala a la presión atmosférica se denomina “Punto de ebullición normal».
Clasificación de la materia
La materia puede clasificarse en dos categorías principales:
Sustancias puras, cada una de las cuales tiene una composición fija y un único conjunto de propiedades.
- Mezclas, compuestas de dos o más sustancias puras.
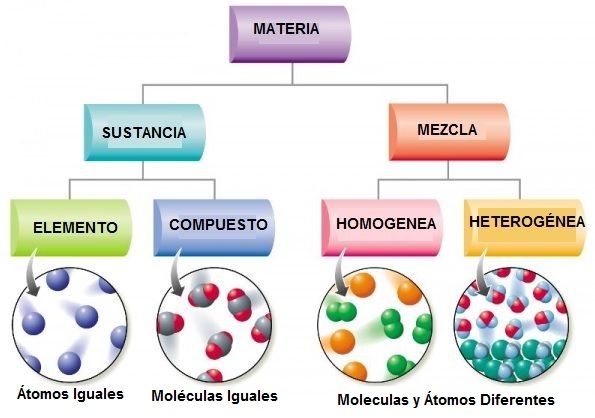
Las sustancias puras pueden ser elementos o compuestos, mientras que las mezclas pueden ser homogéneas o heterogéneas:
- Elemento: Un elemento es un tipo de materia que no puede subdividirse en dos o más sustancias puras. Hay 112 elementos conocidos
- Compuestos: Un compuesto es una sustancia pura que contiene más de un elemento. El agua es un compuesto formado por hidrógeno y oxígeno
- Mezclas homogéneas: Las mezclas homogéneas o uniformes son aquellas en las que la composición es la misma en toda la muestra. La mezcla homogénea también se denomina disolución, que consiste en un disolvente, normalmente la sustancia presente en mayor cantidad, y uno o más solutos.
- Mezclas heterogéneas: Son aquellas en las que la composición de la muestra varía de un punto a otro. Muchas rocas pertenecen a esta categoría. En un trozo de granito se pueden distinguir varios componentes, que se diferencian entre ellos por el color.
Mezclas
Mezclas homogéneas
Mezclas heterogéneas
Una mezcla heterogénea es aquella que posee una composición no uniforme en la cual se pueden distinguir fácilmente sus componentes. Está formada por dos o más sustancias físicamente distintas, distribuidas en forma desigual. Las partes de una mezcla heterogénea pueden separarse fácilmente.
Dispersión coloidal
es un sistema conformado por dos o más fases, normalmente una fluida (líquido o gas) y otra dispersa en forma de partículas generalmente sólidas muy finas, de diámetro comprendido entre 10-9 y 10-5 m. Las partículas coloides tienen propiedades intermedias entre las disoluciones y las suspensiones químicas; se encuentran dispersas sin que estén unidas a las moléculas del disolvente y no se sedimenta al dejarlas en reposo.
Suspensión química
Suspensión se denomina a las mezclas que tienen partículas finas suspendidas en un líquido durante un tiempo y luego se sedimentan. En la fase inicial se puede ver que el recipiente contiene elementos distintos. Se pueden separar por medios físicos. Algunos ejemplos de suspensiones son el engrudo (agua con harina) y la mezcla de agua con aceite.
Tabla con los tipos de mezclas según el estado de agregación de las sustancias
|
Fase disuelta o dispersa |
Medio continuo |
Solución |
Coloide |
Dispersión gruesa |
|
Gas |
Gas |
mezcla de gases: aire (oxígeno y otros gases en nitrógeno) |
Ninguno |
Ninguno |
|
Líquido |
Gas |
Ninguno |
Aerosoles de partículas líquidas: niebla, bruma, vapor, aerosol para el cabello |
Aerosol |
|
Sólido |
Gas |
Ninguno |
Aerosoles de partículas sólidas: humo, nube, partículas en el aire |
Aerosol sólido: polvo |
|
Gas |
Líquido |
Solución: oxígeno en agua |
Espuma líquida: crema batida, crema de afeitar |
Espuma |
|
Líquido |
Líquido |
Solución: bebidas alcohólicas |
Emulsión: miniemulsión, microemulsión |
Emulsión: leche, mayonesa, crema para las manos |
|
Sólido |
Líquido |
Solución: azúcar en agua |
Líquido sol: tinta con pigmentos, sangre |
Suspensión: partículas de barro (tierra, arcilla o limo suspendidas en agua), polvo de tiza suspendido en agua |
|
Gas |
Sólido |
Solución: hidrógeno en metales |
Espuma sólida: aerogel, Poliestireno extruido, piedra pómez |
Espuma: esponja seca |
|
Líquido |
Sólido |
Solución: amalgama (mercurio en oro), hexano en cera parafina |
Gel: agar, gelatina, silicagel, ópalo |
Esponja mojada |
|
Sólido |
Sólido |
Solución: aleaciones, plastificantes en plásticos |
Sol sólido: vidrio rubino oro |
Grava, granito |
Proceso De Separación
 La separación de mezclas es un proceso físico, no químico.
Esto quiere decir que no se constituyen sustancias nuevas luego de la
separación de las mezclas, como sucede en los procesos químicos, donde se
combinan químicamente (se rompen y se forman enlaces químicos) dos o más
sustancias para formar otras nuevas. Existen diferentes métodos entre los que
se destacan la filtración, decantación, destilación, evaporación,
centrifugación, levigación, imantación, lixiviación selectiva, flotación y la
cristalización, entre otros. La elección del método para la separación
dependerá del tipo de mezcla.
La separación de mezclas es un proceso físico, no químico.
Esto quiere decir que no se constituyen sustancias nuevas luego de la
separación de las mezclas, como sucede en los procesos químicos, donde se
combinan químicamente (se rompen y se forman enlaces químicos) dos o más
sustancias para formar otras nuevas. Existen diferentes métodos entre los que
se destacan la filtración, decantación, destilación, evaporación,
centrifugación, levigación, imantación, lixiviación selectiva, flotación y la
cristalización, entre otros. La elección del método para la separación
dependerá del tipo de mezcla.
Algunos métodos de separación de mezclas
Los métodos de separación de mezclas son métodos físicos que se basan en alguna propiedad física de los componentes de la mezcla que se quiere separar, como por ejemplo, el punto de fusión, el punto de ebullición, el estado de agregación, el magnetismo, entre otras.
- Filtración. Se utiliza para separar un sólido de un líquido, siempre que el sólido sea insoluble en el líquido. Se usa un filtro por el que se hace pasar la mezcla, el sólido queda retenido en el filtro y el líquido lo atraviesa.
- Decantación. Se emplea para separar mezclas de dos líquidos insolubles entre sí o mezclas de un
 sólido y un líquido, también insolubles uno en el otro. Para lograr la
separación, la mezcla se deja en reposo en un embudo de decantación, la
sustancia más densa descenderá, mientras que la menos densa quedará en la
superficie. Luego se abre la llave del embudo y se deja pasar a la
sustancia más densa.
sólido y un líquido, también insolubles uno en el otro. Para lograr la
separación, la mezcla se deja en reposo en un embudo de decantación, la
sustancia más densa descenderá, mientras que la menos densa quedará en la
superficie. Luego se abre la llave del embudo y se deja pasar a la
sustancia más densa.
- Destilación. Este método sirve para separar mezclas de líquidos que son solubles entre sí. Está
 basado en las diferencias de puntos de ebullición de los distintos
líquidos. Para separar la mezcla, primero se le aplica calor hasta que el
líquido con menor punto de ebullición pasa a la fase vapor, y se condensa
en otro recipiente. De esta forma queda separado del líquido de mayor
punto de ebullición, que queda solo en el recipiente donde originalmente
estaba la mezcla.
basado en las diferencias de puntos de ebullición de los distintos
líquidos. Para separar la mezcla, primero se le aplica calor hasta que el
líquido con menor punto de ebullición pasa a la fase vapor, y se condensa
en otro recipiente. De esta forma queda separado del líquido de mayor
punto de ebullición, que queda solo en el recipiente donde originalmente
estaba la mezcla.
- Centrifugación. Se emplea generalmente para separar un sólido insoluble en un líquido. La amezcla se hace girar en una centrífuga (un recipiente que gira), provocando que la fuerza centrífuga envíe el sólido hacia el fondo del recipiente y dejando el líquido en la parte superior. Luego pueden separarse empleando decantación.
- Levigación. Se utiliza
para separar mezclas de sólidos. Se trituran los sólidos y se les añade undisolvente. Luego esta nueva mezcla se puede separar según las distintas
densidades de sus componentes.
- Imantación. Consiste en
separar una mezcla de sustancias en la que al menos una de ellas tiene
propiedades magnéticas y puede ser atraída por un imán.
- Lixiviación selectiva. Es un método que emplea distintos disolventes para separar una mezcla. Cada componente de la mezcla tendrá más afinidad por un disolvente específico, por lo que al poner en contacto cada disolvente con la mezcla se separará el componente más afín con él. Este proceso es muy utilizado en la minería para extraer oro.
Ley de conservación de la materia
O También llamada ley de Lomonósov-Lavoisier es una ley fundamental de las ciencias naturales. Fue elaborada independientemente por Mijaíl Lomonósov en 1748 y descubierta unos años después por Antoine Lavoisier en 1785. Dice: «En un sistema aislado, durante toda reacción química ordinaria, la masa total en el sistema permanece constante, es decir, la masa consumida de los reactivos es igual a la masa de los productos obtenidos».
La ley implica que la masa no se puede crear ni destruir, pero puede transformarse en el espacio, o las entidades asociadas con ella pueden cambiar de forma. Por ejemplo, en las reacciones químicas, la masa de los componentes químicos antes de la reacción es igual a la masa de los componentes después de la reacción. Por lo tanto, durante cualquier reacción química y procesos termodinámicos de baja energía en un sistema aislado, la masa total de los reactivos o materiales de partida debe ser igual a la masa de los productos
Ley de las proporciones constantes
es una de las leyes estequiométricas, según la cual cuando se combinan dos o más elementos para dar un determinado compuesto, siempre lo hacen en una relación constante de masas. Enunciada por el farmacéutico y químico francés Louis Proust, basándose en experimentos que llevó a cabo a principios del siglo XIX; por lo tanto, también se conoce como la ley de Proust.
Para los compuestos que la siguen, por tanto, la proporción de masas entre los elementos que los forman es constante. En términos más modernos de la fórmula molecular, esta ley implica que siempre se van a poder asignar subíndices fijos a cada compuesto.Hay que notar que existe una clase de compuestos, denominados compuestos no estequiométricos (también llamados bertólidos), que no siguen esta ley. Para estos compuestos, la razón entre los elementos puede variar continuamente entre ciertos límites. Naturalmente, otros materiales como las aleaciones o los coloides, que no son propiamente compuestos sino mezclas, tampoco siguen esta ley.
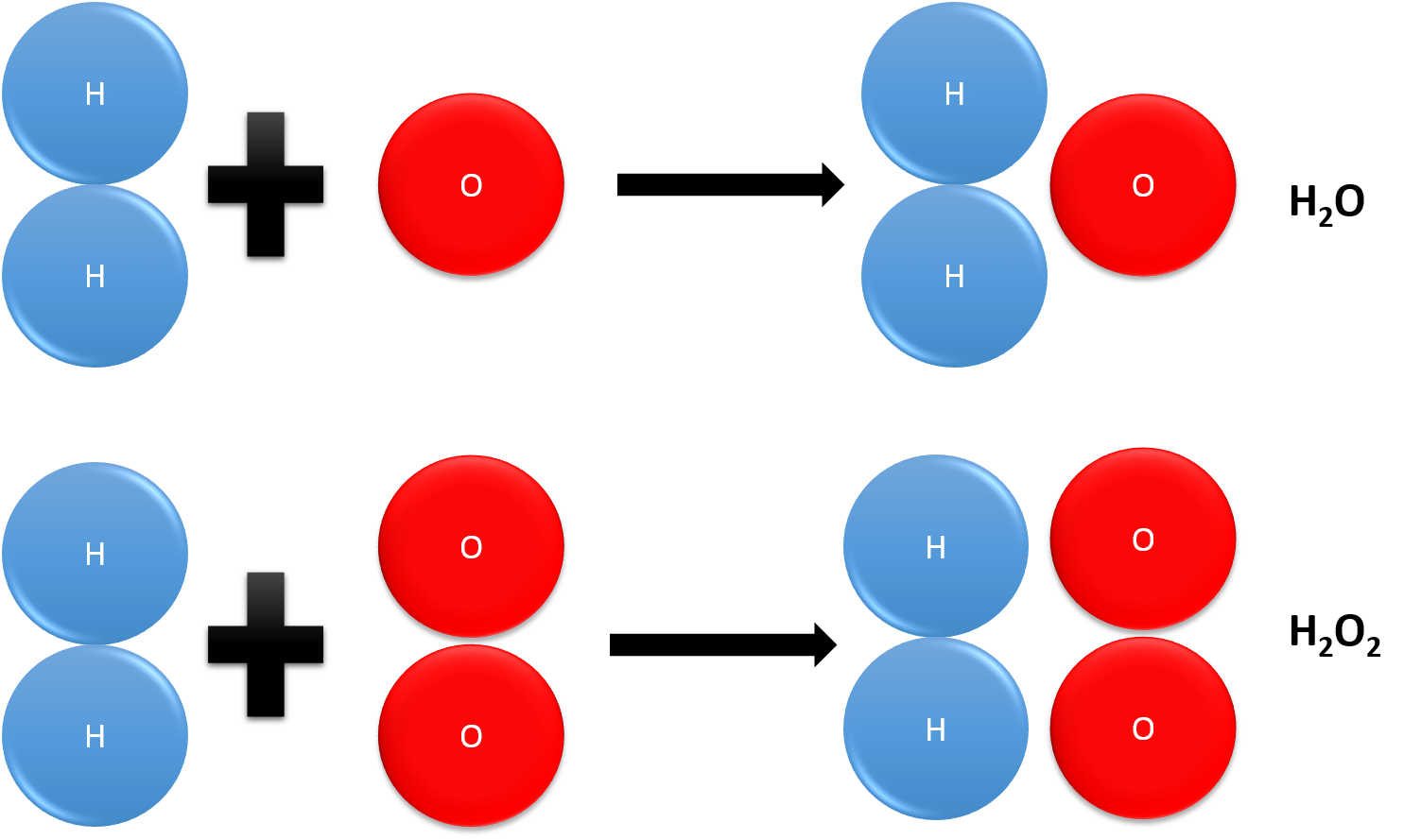
Ley de las proporciones múltiples
John Dalton expresó por primera vez esta observación en 1804. Unos años antes, el químico francés Joseph Proust había propuesto la ley de las proporciones definidas, que expresaba que los elementos se combinaban para formar compuestos en ciertas proporciones bien definidas, en lugar de mezclarse en cualquier proporción; y Antoine Lavoisier demostró la ley de conservación de la masa, que ayudó a Dalton. Un cuidadoso estudio de los valores numéricos reales de estas proporciones llevó a Dalton a proponer su ley de las proporciones múltiples. Este fue un paso importante hacia la teoría atómica que propondría ese mismo año, y sentó las bases de las fórmulas químicas de los compuestos.
 |
| oligómeros |
 | |
| Polimero |
Análisis
Conclusión
Bibliografía
- Química. (2022, 29 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:08, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Qu%C3%ADmica&oldid=143212116.
- Cueva de Blombos. (2021, 25 de agosto). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:09, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Cueva_de_Blombos&oldid=137907788.
- Anexo:Cronología de la química. (2022, 2 de marzo). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:09, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Anexo:Cronolog%C3%ADa_de_la_qu%C3%ADmica&oldid=142028710.
- Alquimia. (2022, 1 de mayo). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:09, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Alquimia&oldid=143253098.
- Historia de la química. (2022, 17 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:10, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Historia_de_la_qu%C3%ADmica&oldid=142945614.
- Electrón. (2022, 21 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:10, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Electr%C3%B3n&oldid=143040636.
- Materia. (2022, 30 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 19:12, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Materia&oldid=143232929.
- Materia. (2021, 15 de julio). Autor: Dianelys Ondarse Álvarez. De: Argentina. Para: Concepto.de. Fecha de consulta: 19:15, mayo 2, 2022 desde Disponible en: https://concepto.de/materia/.
- Clasificación de la materia. CNICE. Fecha de consulta: 19:17, mayo 2, 2022 desde: http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/clasif/clasifica1.htm
- Coloide. (2022, 28 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 23:41, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Coloide&oldid=143196964.
- Mezcla. (2022, 24 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 23:42, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Mezcla&oldid=143113272.
- Proceso de separación. (2021, 17 de octubre). Wikipedia, La enciclopedia libre. Fecha de consulta: 23:42, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Proceso_de_separaci%C3%B3n&oldid=139107227.
- "Separación de mezclas". Autor: Julia Máxima Uriarte. Para: Caracteristicas.co. Última edición: 30 de septiembre de 2021. Fecha de consulta: mayo 2, 2022 Disponible en: https://www.caracteristicas.co/separacion-de-mezclas/.
- Ley de conservación de la materia. (2022, 25 de marzo). Wikipedia, La enciclopedia libre. Fecha de consulta: 23:44, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Ley_de_conservaci%C3%B3n_de_la_materia&oldid=142488346.
- Ley de las proporciones constantes. (2022, 10 de marzo). Wikipedia, La enciclopedia libre. Fecha de consulta: 23:44, mayo 2, 2022 desde https://es.wikipedia.org/w/index.php?title=Ley_de_las_proporciones_constantes&oldid=142197908.
- Colaboradores de Wikipedia. (2021, 26 de septiembre). Law of multiple proportions. En Wikipedia, La Enciclopedia Libre. Consultado el 23:45, 2 de mayo de 2022, desde https://en.wikipedia.org/w/index.php?title=Law_of_multiple_proportions&oldid=1046611062
- Clorofluorocarburo. (2022, 25 de abril). Wikipedia, La enciclopedia libre. Fecha de consulta: 01:39, mayo 4, 2022 desde https://es.wikipedia.org/w/index.php?title=Clorofluorocarburo&oldid=143128498.









.png)









Comentarios
Publicar un comentario